Farmacología

Aumento en las dosis de inhibidores de la bomba de protones: ¿un truco de magia?
18 marzo 2026
Revisión sistemática de ensayo clínicos aleatorizados, comparativos cabeza a cabeza. El objetivo fue comprobar si los medicamentos de "molécula única" (los que tienen "dex" o "es" en su nombre, como el dexlansoprazol o el esomeprazol) realmente funcionan mejor que las versiones originales y más económicas (lansoprazol u omeprazol). Los investigadores concluyen que no se deben prescribir inhibidores de la bomba de protones (IBP) en dosis altas durante muchos años hasta que se disponga de mejores pruebas de seguridad a largo plazo. Prescribir omeprazol o lansoprazol en lugar de enantiómeros individuales podría suponer un ahorro de más de 21 millones de dólares anuales en la Columbia Británica, con la posibilidad de obtener ahorros adicionales significativos al cambiar a pantoprazol. Therapeutics letter, 12 de marzo de 2026

Psicofármacos en Pediatría
18 marzo 2026
El uso de psicofármacos en niños y adolescentes ha experimentado un crecimiento notable en las últimas décadas, impulsado por una mayor detección de trastornos mentales y avances en la investigación clínica. El artículo subraya que el tratamiento farmacológico en pediatría debe entenderse siempre como parte de un abordaje terapéutico integral, que incluya intervenciones psicosociales, apoyo familiar y adaptaciones pedagógicas; nunca debe ser la única modalidad de tratamiento. An Pediatr (Barc). marzo de 2026
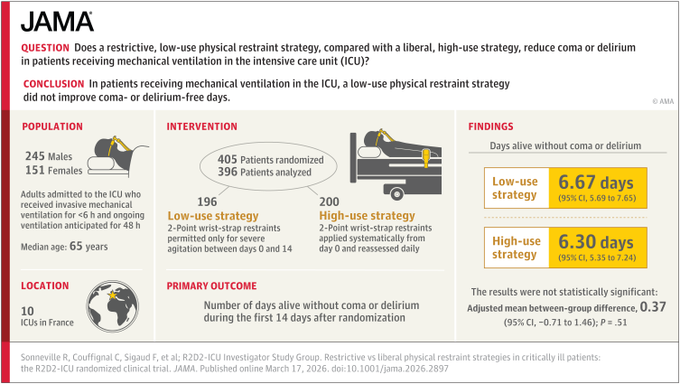
Estrategias de contención física restrictivas frente a liberales en pacientes críticos: ensayo clínico aleatorizado R2D2-ICU.
18 marzo 2026
El delirio y el coma son complicaciones frecuentes y graves para los pacientes en la unidad de cuidados intensivos (UCI) que reciben ventilación mecánica. A menudo se utilizan sujeciones físicas, como las muñequeras, para prevenir autolesiones, pero no está claro si un enfoque de bajo uso mejora los resultados.Este ensayo investigó si una estrategia de sujeción física restrictiva con correas de muñeca de bajo uso reduce el coma o el delirio en pacientes adultos que reciben ventilación mecánica en la unidad de cuidados intensivos (UCI) en comparación con una estrategia más liberal y de alto uso. Se encontró que una estrategia de sujeción física con correas de muñeca de bajo uso, en comparación con una estrategia de alto uso, no redujo los días libres de delirio o coma a los 14 días. JAMA, 17 de marzo de 2026.

Guía de 2026 sobre el manejo de la dislipidemia: Informe del Comité Conjunto del Colegio Americano de Cardiología/Asociación Americana del Corazón
18 marzo 2026
La “Guía de 2026 sobre el manejo de la dislipidemia” de la ACC/AHA/AACVPR/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA reemplaza a la “Guía 2026 sobre el Manejo de la Dislipidemia”. El objetivo de la guía es abordar de forma práctica la evaluación, el manejo y el seguimiento de pacientes con dislipidemias, incluyendo colesterol alto, hipertrigliceridemia y lipoproteína (a) elevada [Lp(a)]. Esta guía, se ha modificado para reflejar la comprensión en constante evolución del riesgo de ECVA asociado a lipoproteínas aterogénicas más allá de las partículas LDL, incluyendo TG y partículas remanentes, y Lp(a). J Am Coll Cardiol. 13 de marzo de 2026

Nuevos tratamientos emergentes para los trastornos de ansiedad
18 marzo 2026
