Farmacología

Aprobación de gabapentina, uso fuera del prospecto y lecciones para realizar esfuerzos de evaluación posteriores a la comercialización
28 febrero 2018
JAMA, 27 de febrero de 2018 25 años después de la aprobación inicial de la gabapentina, tiene 3 indicaciones aprobadas en EE.UU., pero es el séptimo fármaco más prescrito en ese país. (una evaluación en personas asistidas por Medicaid estimó que el 95% fue para indicaciones no aprobadas
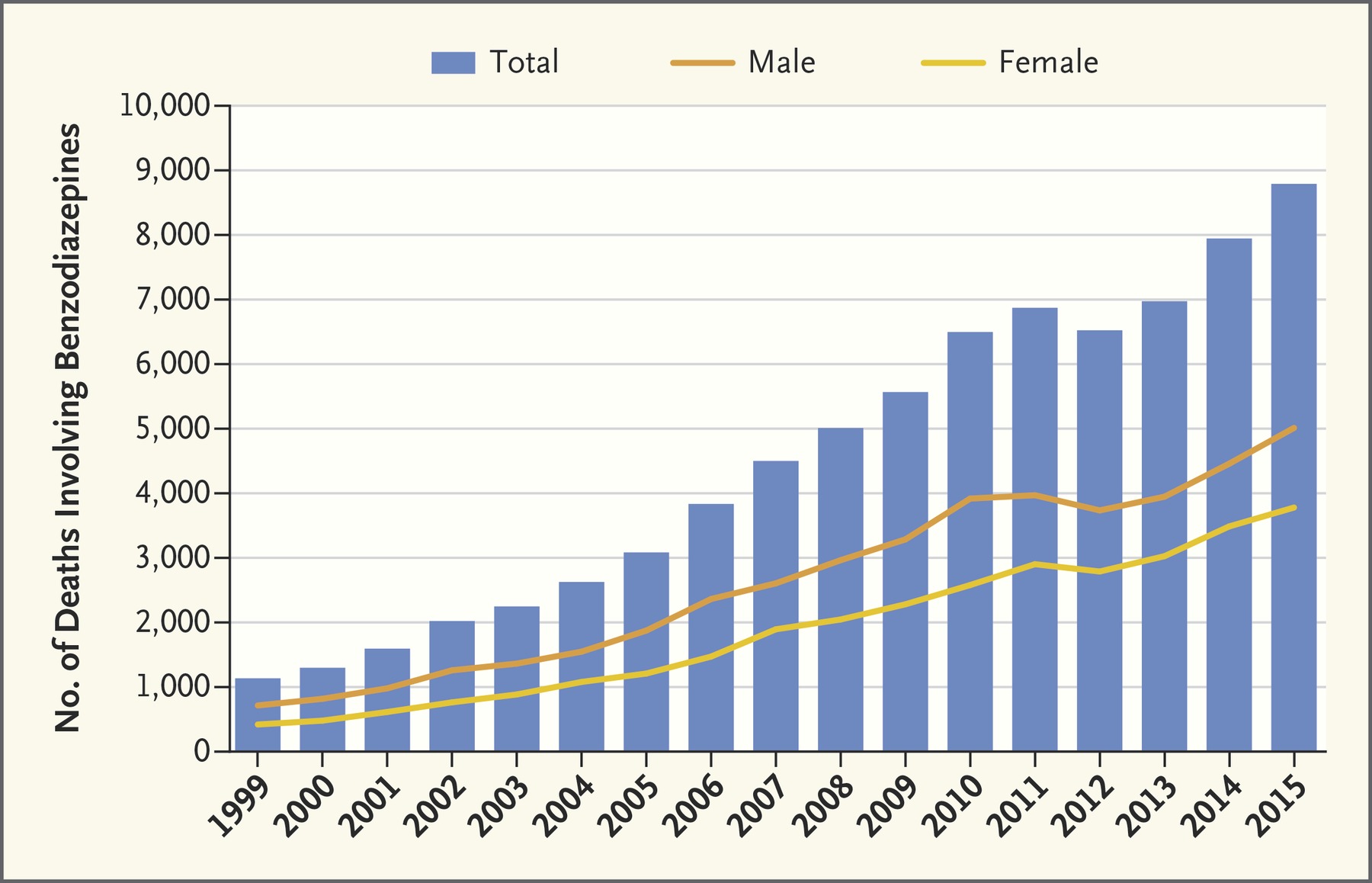
Benzodiacepinas, otro grupo de medicamentos problemático
26 febrero 2018
N Engl J Med, 22 de febrero de 2018 Las benzodiazepinas tienen una utilidad comprobada cuando se usan intermitentemente y por menos de 1 mes. Pero cuando se usan a diario y durante períodos prolongados, los beneficios de las benzodiazepinas disminuyen y los riesgos asociados con su uso aumentan.

Sacubitrilo-Valsartán en insuficiencia cardiaca: evaluación crítica del ensayo Paradigm-HF
26 febrero 2018
BIT Navarra: Volumen 25, número 3 Servicio Navarro de Salud-Osasunbidea, 26 de febrero de 2018 Por motivos de eficacia y seguridad, se debe seleccionar de forma exquisita aquel paciente que más se pueda beneficiar del tratamiento con SAC/VAL que, por el momento, no puede considerarse de primera elección en la ICC.
Comparación de nuevos medicamentos aprobados por la FDA, la EMA y Swissmedic: una evaluación de la armonización internacional de drogas
26 febrero 2018
Eur J Clin Pharmacol, 22 de febrero de 2018 Hubo diferencias en las características de los nuevos medicamentos aprobados por la EMA, la FDA y SMC en el período 2007-2016. En general, dos tercios de los nuevos medicamentos fueron aprobados por primera vez por la FDA. Las diferencias en las indicaciones se encontraron en tres de cuatro nuevos medicamentos aprobados por las tres agencias reguladoras. A pesar de los esfuerzos internacionales de armonización de la regulación de medicamentos, persisten diferencias significativas en las características de los nuevos medicamentos aprobados por diferentes agencias.

FDA. Claritromicina (Biaxin): riesgo potencial aumentado de problemas cardíacos o muerte en pacientes con enfermedad cardíaca
23 febrero 2018
