Farmacología

Características y confirmación posterior de las alertas de seguridad notificadas a la FDA
06 octubre 2022
La mayoría de las posibles señales de seguridad identificadas condujeron a la adopción de medidas reglamentarias por parte de la FDA. Sin embargo, solo un tercio de las acciones regulatorias fueron corroboradas por investigaciones publicadas y ninguna por evaluaciones públicas de la Iniciativa Sentinel. Estos hallazgos sugieren que, o bien la FDA está tomando medidas reglamentarias basadas en pruebas que no se han puesto a disposición del público, o que podrían ser necesarias evaluaciones de seguridad más exhaustivas cuando se identifiquen posibles señales de seguridad. British Medical Journal, 5 de octubre de 2022.
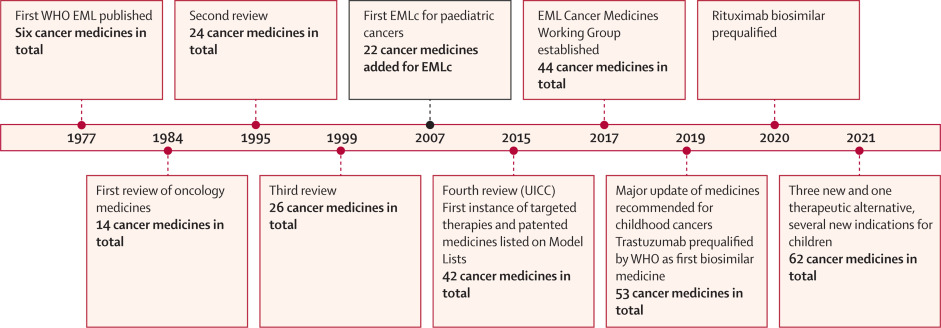
Medicamentos contra el cáncer en la Lista Modelo de Medicamentos Esenciales de la OMS: procesos, desafíos y camino a seguir
30 septiembre 2022
Este documento de política de salud describe cómo se enumeran los medicamentos contra el cáncer en la EML y la EMLc, incluidos dos procesos actualizados de la OMS: (1) la formación del Grupo de trabajo sobre medicamentos contra el cáncer y (2) principios de selección adicionales para recomendar medicamentos contra el cáncer, incluido un beneficio mínimo de supervivencia general de 4 a 6 meses con una mejora en la calidad de vida en comparación con el tratamiento estándar. Lancet Glob Health, 29 de septiembre de 2022

Responsabilidad de los ejecutivos por actividades ilegales de empresas farmacéuticas y de dispositivos médicos
28 septiembre 2022
Estos hallazgos sugieren que el gobierno no ha ejercido todo el alcance de su autoridad para enjuiciar a los funcionarios corporativos responsables del comportamiento ilegal de las compañías de medicamentos y dispositivos que dirigen. La aplicación bajo una doctrina Park revitalizada podría promover mejor el objetivo de la doctrina de proteger a los pacientes. JAMA Intern Med. 19 de septiembre de 2022.

Declaración sobre los fundamentos científicos que respaldan la intercambiabilidad de los medicamentos biosimilares en la Unión Europea (UE)
21 septiembre 2022
Los expertos de la UE en medicamentos biosimilares (Grupo de Trabajo de Medicamentos Biosimilares o BMWP) y el Grupo de Trabajo de Biosimilares de los Jefes de Agencias de Medicamentos (HMA) han redactado una declaración conjunta que explica los fundamentos para considerar biosimilares aprobados en la UE como intercambiables desde una perspectiva científica. EMA, 19 de septiembre de 2022

Medicamentos retirados en otros países por problemas de seguridad¿Deben seguir presentes en el mercado farmacéutico argentino?
16 septiembre 2022
